Rūgštys ir bazės yra dvi pagrindinės cheminių junginių grupės, pasižyminčios priešingomis savybėmis. Sumaišius rūgštį su baze, įvyksta cheminė reakcija, vadinama neutralizacija.
Neutralizacijos reakcija
Neutralizacijos reakcijos metu rūgštis ir bazė reaguoja tarpusavyje, sudarydamos druską ir vandenį.
Bendroji neutralizacijos reakcijos lygtis:
Rūgštis + Bazė → Druska + Vanduo
Pavyzdžiui, sumaišius druskos rūgštį (HCl), kuri yra rūgštis, su natrio hidroksidu (NaOH), kuris yra bazė, susidaro natrio chloridas (NaCl), arba valgomoji druska, ir vanduo (H₂O):
HCl + NaOH → NaCl + H₂O
Šioje reakcijoje rūgšties vandenilio jonai (H⁺) reaguoja su bazės hidroksido jonais (OH⁻), sudarydami vandenį. Likę jonai (Cl⁻ ir Na⁺) sudaro druską.
Reakcijos pasekmės
Neutralizacijos reakcijos metu rūgšties ir bazės savybės išnyksta. Susidaręs tirpalas tampa neutralus, t. y., jo pH lygus 7. pH skalė naudojama rūgštingumui arba bazingumui matuoti. pH mažesnis nei 7 rodo rūgštinę terpę, didesnis nei 7 - bazinę, o lygus 7 - neutralią.
Neutralizacijos reakcijos metu dažnai išsiskiria šiluma. Tokios reakcijos vadinamos egzoterminėmis. Išsiskyrusios šilumos kiekis priklauso nuo rūgšties ir bazės stiprumo.
Praktinis pritaikymas
Neutralizacijos reakcijos plačiai naudojamos įvairiose srityse:
- Rūgštingumo mažinimas dirvožemyje: kalkės (kalcio karbonatas) naudojamos dirvožemio rūgštingumui mažinti.
- Skrandžio rūgštingumo mažinimas: antacidai, kurių sudėtyje yra bazių, naudojami skrandžio rūgštingumui mažinti.
- Pramonė: neutralizacijos reakcijos naudojamos atliekų vandens valymui ir cheminių medžiagų gamybai.
Svarbu žinoti
Maišant rūgštis ir bazes, būtina laikytis atsargumo priemonių, nes reakcija gali būti labai energinga ir sukelti pavojų. Visada reikia naudoti apsaugines priemones, tokias kaip akiniai ir pirštinės, ir maišyti medžiagas lėtai bei atsargiai.
Stiprios rūgštys ir bazės
Stiprios rūgštys ir bazės visiškai disocijuoja vandenyje, todėl reakcijos su jomis yra labai greitos ir išskiria daug šilumos. Maišant stiprias rūgštis ir bazes, reikia būti ypač atsargiems.
Silpnos rūgštys ir bazės
Silpnos rūgštys ir bazės disocijuoja vandenyje tik iš dalies, todėl reakcijos su jomis yra lėtesnės ir išskiria mažiau šilumos.
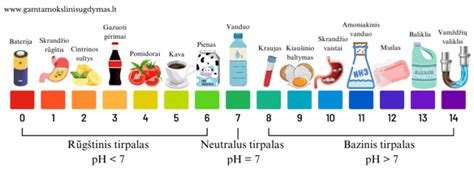
pH skalė
Neutralizacijos svarba
Neutralizacija yra gyvybiškai svarbi reakcija, kuri užtikrina stabilumą daugelyje biologinių ir cheminių procesų. Ji padeda palaikyti pastovų pH lygį organizmuose ir aplinkoje.
| Rūgštis | Bazė | Druska | Pavyzdys |
|---|---|---|---|
| Druskos rūgštis (HCl) | Natrio hidroksidas (NaOH) | Natrio chloridas (NaCl) | HCl + NaOH → NaCl + H₂O |
| Sieros rūgštis (H₂SO₄) | Kalio hidroksidas (KOH) | Kalio sulfatas (K₂SO₄) | H₂SO₄ + 2KOH → K₂SO₄ + 2H₂O |
Ši lentelė iliustruoja, kaip įvairios rūgštys ir bazės reaguoja, sudarydamos atitinkamas druskas ir vandenį.
Išvados
Sumaišius rūgštį su baze, įvyksta neutralizacijos reakcija, kurios metu susidaro druska ir vanduo. Ši reakcija yra labai svarbi ir plačiai naudojama įvairiose srityse. Svarbu prisiminti, kad maišant rūgštis ir bazes, būtina laikytis atsargumo priemonių.